I. PrehľadESMOUsmernenie z roku 2025
V auguste 2025 ESMO oficiálne vydalo dokument Včasný a lokálne pokročilý nemalobunkový karcinóm pľúc: Klinická prax ESMO pre diagnostiku, liečbu a sledovanie, ktorý bol publikovaný v poprednom onkologickom časopise Annals of Oncology. Ide o prvú komplexnú aktualizáciu od verzie z roku 2017 a poskytuje mimoriadne autoritatívny referenčný materiál pre onkológov na celom svete.

Rakovina pľúc má celosvetovo najvyšší výskyt a úmrtnosť zo všetkých malignít. Každý rok sa objaví viac ako 2,2 milióna nových prípadov a viac ako 1,8 milióna úmrtí, čo robí z rakoviny pľúc hlavnú príčinu úmrtí súvisiacich s rakovinou u mužov aj žien. Nemalobunkový karcinóm pľúc (NSCLC) predstavuje približne 80 – 85 % všetkých pacientov s rakovinou pľúc. Vzhľadom na túto vážnu situáciu prináša vydanie usmernenia z roku 2025 nový vedecký impulz do klinickej praxe, pričom aktualizácia stratégií testovania biomarkerov je obzvlášť dôležitá.
II. Interpretácia aktualizácií kľúčových usmernení
2.1 Testovanie biomarkerov: Od „voliteľného“ po „nevyhnutné“
Usmernenie z roku 2025 predstavuje míľnikovú strategickú úpravu týkajúcu sa testovania biomarkerov. Usmernenie výslovne uvádza, že testovanie biomarkerov je nevyhnutné pre rozhodnutie o liečbe u pacientov s NSCLC v štádiu IB-III.“
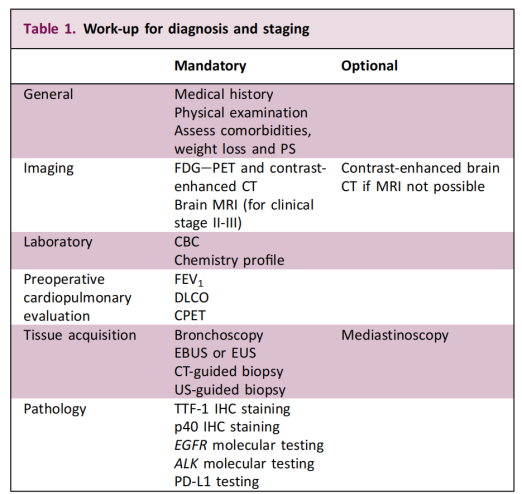
Toto odporúčanie rozširuje molekulárne testovanie z jeho predchádzajúceho zamerania na pacientov s pokročilým ochorením na prípady v ranom štádiu, ktoré je možné resekovať. Hlavným cieľom je identifikovať mutácie hnacieho génu a poskytnúť vedecký základ pre personalizovanú a presnú liečbu. Usmernenie tiež zdôrazňuje, že uskutočniteľnosť biopsie a diagnostický prístup by mal určiť multidisciplinárny tím na základe charakteristík pacienta a nádoru.
Pokiaľ ide o špecifickú stratégiu testovania, usmernenie jasne odporúča, aby sa genetické testovanie vykonalo pred rozhodnutím o chirurgickom zákroku a aby zahŕňalo aspoň EGFR a ALK. Tento koncept „testovania vopred“ má hlboký klinický význam pre presnú stratifikáciu a personalizovanú liečbu NSCLC v ranom štádiu – včasnosť a presnosť výsledkov testov priamo určujú výber následnej adjuvantnej liečby.
2.2 Terapeutické objavy v liečbe NSCLC v ranom štádiu s pozitívnym driver-onkogénom
Usmernenie z roku 2025 integruje dôkazy z viacerých významných klinických štúdií s cieľom stanoviť jasný a presný liečebný postup pre pacientov s NSCLC v ranom štádiu s pozitívnym driver-onkogénom.
Pacienti s pozitívnou mutáciou EGFR:Na základe prelomovej štúdie ADAURA sa pooperačná adjuvantná liečba osimertinibom počas troch rokov stala globálnym štandardom starostlivosti o pacientov s deléciami exónu 19 EGFR alebo mutáciami L858R exónu 21. Štúdia ADAURA je medzinárodná, multicentrická, randomizovaná, kontrolovaná štúdia fázy III, ktorá hodnotí účinnosť a bezpečnosť adjuvantnej liečby osimertinibom u pacientov s kompletne resekovaným NSCLC v štádiu IB-IIIA s mutáciou EGFR. Štúdia preukázala, že osimertinib významne zlepšil prežívanie bez ochorenia aj celkové prežívanie v porovnaní s placebom, čím sa osimertinib stal novým štandardom starostlivosti pre túto populáciu. Exploratívna analýza štúdie ADAURA však ukázala, že približne 36 % predčasného ukončenia liečby bolo spôsobených nežiaducimi udalosťami a ďalších 31 % bolo spôsobených rozhodnutím pacienta. Toto zistenie zdôrazňuje potrebu presného východiskového testovania pred liečbou, aby sa zabezpečilo, že cielená liečba sa podáva pacientom, ktorí môžu mať z liečby trvalý úžitok.
ALK-pozitívni pacienti:Na základe štúdie ALINA je v súčasnosti štandardom starostlivosti pooperačný adjuvantný alektinib počas dvoch rokov. V primárnej analýze randomizovanej otvorenej štúdie ALINA fázy III preukázal alektinib výrazný prínos v prežívaní bez ochorenia v populácii v štádiu II-IIIA s pomerom rizika 0,24. Aktualizované údaje zo štúdie ALINA prezentované na kongrese ESMO 2025 ukázali, že po ≥3 rokoch sledovania zostal prínos alektinibu pre prežívanie bez ochorenia „trvalý a klinicky významný“ s pomerom rizika 0,36 v populácii v štádiu II-IIIA. Najnovšie hlásená celková miera prežitia po 4 rokoch dosiahla 98,4 %, miera prežívania bez ochorenia po 4 rokoch bola 75,5 % a zlepšilo sa aj prežívanie bez ochorenia centrálneho nervového systému bez akýchkoľvek nových bezpečnostných signálov. Tieto robustné údaje ďalej potvrdzujú, že adjuvantný alektinib je štandardom starostlivosti po resekcii ALK-pozitívneho NSCLC a zdôrazňujú dôležitosť presného testovania na identifikáciu takýchto pacientov.
Výber testovacej metódy:V usmernení ESMO z roku 2025 sa výslovne uvádzamultiplexné RT-PCR panelové testypopri NGS na báze RNA, IHC a FISH ako jeden z odporúčaných technických prístupov na detekciu fúzie ALK. To naznačuje, že základnou požiadavkou smernice je vykonávať testovanie na usmernenie klinických rozhodnutí, a nie nariaďovať konkrétnu testovaciu platformu. V prípade produktov RT-PCR zameraných na detekciu EGFR a ALK táto flexibilná testovacia stratégia poskytuje silné odôvodnenie ich použitia v klinickej praxi založené na smerniciach.
III. Technické riešenia pre presné testovanie
Smernica z roku 2025 posúva testovanie do fázy predoperačného rozhodovania, čo zvyšuje latku presnosti, citlivosti a dostupnosti testov. Dva detekčné produkty založené na RT-PCR opísané nižšie presne zodpovedajú požiadavkám smernice z technického hľadiska.
3.1 Súprava na detekciu mutácií EGFR – vylepšená technologická platforma ARMS
Základná technológiaVylepšená technológia ARMS umožňuje špecifickú amplifikáciu mutantných sekvencií s nízkou abundanciou oproti vysokému pozadiu divokého typu
Tri technické záruky:
-Vylepšený ARMS → zlepšuje rozpoznávanie mutácií
-Enzymatické obohatenie → štiepi pozadie divokého typu a obohacuje mutantné sekvencie
-Blokovanie teplotou → potláča nešpecifickú amplifikáciu
VýkonCitlivosť1 % frekvencia mutantných alel
Kontrola kontaminácieVstavaná vnútorná kontrola + enzým UNG zabraňujú kontaminácii
Doba spracovaniaPrevádzka v uzavretej trubici, približne120 minút
Kompatibilita vzoriek:Tkanivo/tekutá biopsiavzorky → rieši požiadavku „predbežného testovania“
Pokrytie:45 mutáciív exónoch 18-21 EGFR, presne zodpovedajúce oblasti zvýraznené podľa pokynov (delécie exónu 19 a exónu 21 L858R)
Klinické použitiePriamo riadi terapiu EGFR-TKI
3.2 Súprava na detekciu fúzie MMT EML4-ALK – roztok na detekciu fúzie na báze RNA

-Technologická platformaRT-PCR na báze RNA – ponúka inherentné výhody oproti metódam založeným na DNA na detekciu fúzií
-Výhoda založená na RNAPriamo detekuje exprimované fúzne transkripty, čím účinne zabraňuje falošne negatívnym výsledkom
-Dôkazy zo štúdiePri fúziách ALK s nízkym výskytom je RT-PCR výrazne spoľahlivejšia ako testy založené na DNA.
-CitlivosťDetekuje fúzie až do20 kópií na reakciu
-Pokrytie variantovKryty12 bežných fúznych variantov EML4-ALK(vrátane variantu 1 ~33 %; varianty 3a/3b spolu ~29 %)
-Prevádzka a kontrola kontaminácieUzavretá skúmavka, ~120 minút; vstavané kontroly procesu + enzým UNG zabraňujú falošným výsledkom
-Kompatibilita prístrojovKompatibilné s rôznymi bežnými prístrojmi pre PCR v reálnom čase
-Zarovnanie vodiacej čiaryVysoko v súlade s usmerneniami ESMO
IV. Súlad medzi testami a odporúčaniami v usmerneniach
Tieto dva detekčné produkty sú vo vysokej miere v súlade s usmerneniami ESMO 2025 pre včasný a lokálne pokročilý nemalobunkový karcinóm pľúc v nasledujúcich kľúčových aspektoch:
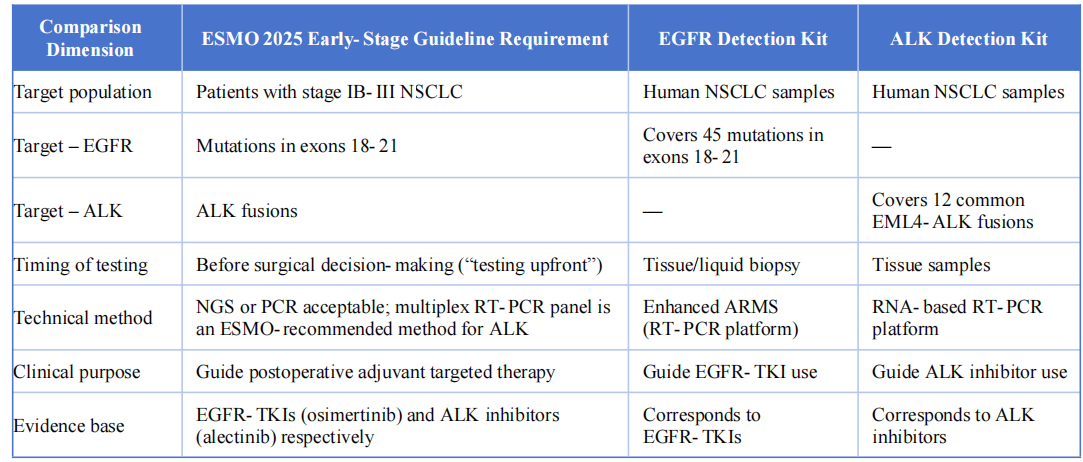
V. Záver
Usmernenie ESMO 2025 pre včasný štádium NSCLC oznamuje novú éru presnej diagnostiky a liečby zameranej na „testovanie vopred, presné zacielenie a optimalizácia liečby.„Súprava na detekciu mutácií EGFR a súprava na detekciu fúzie MMT EML4-ALK spĺňajú požiadavky smernice na ciele, načasovanie a presnosť prostredníctvom odlišných technických ciest.“
Súprava EGFR využíva vylepšenú technológiu ARMS na vysoko citlivú detekciu cielených mutácií v obmedzených vzorkách, pričom podporuje biopsiu tkaniva aj tekutiny, aby umožnila „testovanie vopred“.
Súprava ALK je založená na RNA RT-PCR, ktorá ponúka oproti DNA metódam detekcie fúzií výhody, čo je v súlade s odporúčaním ESMO pre multiplexné RT-PCR panely na testovanie ALK.
Tieto dva produkty spolu tvoria presné testovacie riešenie, ktoré je v súlade s usmernením ESMO 2025 a podporuje personalizovanú adjuvantnú terapiu pre NSCLC v ranom štádiu.
Referencie:
- Zer A, Ahn MJ, Barlesi F a kol. Včasný a lokálne pokročilý nemalobunkový karcinóm pľúc: Klinická prax ESMO pre diagnostiku, liečbu a sledovanie. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Čas uverejnenia: 06.05.2026

